محتويات

التفاعل الكيميائي
التفاعل الكيميائيُّ هو عملية تغيير الخصائص الفيزيائية والكيميائية للمواد المتفاعلة، وإنتاج مواد جديدة بخصائص فيزيائيّة وكيميائيّة مُختلفة من خلال تكسير روابط في المواد المُتفاعلة لإنتاج روابط جديدة في المواد الناتجة، وتحدث التفاعلات الكيميائيّة إمّا باتحاد بعض الجزيئات بطرق مُختلفة لتكوين مُركّبات أكبر وأكثر تعقيداً، أو بتفكُّك بعض الجزيئات لتكوين جزيئات أصغر، وأما بإعادة ترتيب الذرات في المركب، وتخضع التفاعلات الكيميائية لقانون حفظ الكتلة؛ الذي ينص على أنّه عند حدوث أيّ تفاعل كيميائي فإن كتل المواد الداخلة في التفاعل تساوي كتل المواد الناتجة منه؛ أيّ أنّ المادة في نظام مغلق لا يُمكن أن تنشأ أو تَفنى إلا أنّه يُمكن إعادة ترتيبها.
توضيح التعريف
سنعرض التفاعل التالي كمثال لتوضيح مفهوم التفاعل الكيميائي:
2Na + CL2 → 2NaCL
نلاحظ في هذا المثال تفاعل غاز الكلور مع عنصر الصوديوم لإنتاج مركب كلوريد الصوديوم (ملح الطعام) ونستنتج أنّ:
- خصائص المواد الناتجة من التفاعل الكيميائي تختلف عن خصائص المواد المتفاعلة، بحيث أنّ غاز الكلور سامّ، وله لونٌ أصفر مُخضرّ، ومادة الصوديوم ليّنة وسهلة القطع، وملح الطعام الناتج يذوب في الماء، ومحلوله المائيُّ الناتج يوصل التيار الكهربائي، كما أنّه يُعدّ ضرورياً على موائد الطعام.
- لا تتغير كتلة المواد المتفاعلة بعد حدوث التفاعل؛ حيث إنّ كتلة غاز الكلور والصوديوم تساوي كتلة كلوريد الصوديوم الناتج، أيّ أن: كتلة المواد المتفاعلة=كتلة المواد الناتجة.
أنواع التفاعلات الكيميائية
- اتحاد مباشر.
- تحلل كيميائي.
- تفاعل استبدال أحادي.
- تفاعل استبدال ثنائي.
- احتراق.
- تفاعلات عضوية.
- تفاعلات تامّة.
- تفاعلات انعكاسيّة.
دلالات حدوث التفاعلات الكيميائية
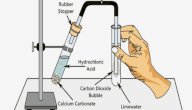
- تصاعد غاز، مثال: Zn+2HCl→ZnCl2+ H2
- تتفاعل مادة الخارصين في محلول حمض الهيدروكلوريك، فينتج كلوريد الخارصين، ويتصاعد غاز الهيدروجين.
- اختفاء اللون، مثال: يمتلك الهكسين (C6H12) اللون الأحمر، ولكن عند تفاعله مع البروم يختفي لونه وينتج مركب عديم اللون.
- ظهور لون جديد، مثال: عند تفاعل اليود مع النشا، تنتج مادة ذات لون أزرق.
- التغيُّر في درجة الحرارة، مثال: عند إضافة حمض الهيدروكلوريك (HCL) إلى محلول هيدروكسيد الصوديوم (NaOH)، تتغير درجة حرارتهما.
- ظهور راسب، مثال: AgNO3+NaCl→AgCl+NaNO3
- يظهر كلوريد الفضة AgCl كراسب نتيجة تفاعل نترات الفضة AgNO3 مع كلوريد الصوديوم NaCl
- سريان التيار الكهربائي، مثال: إذا وُصل قطبا مصباح صغير بقضيبي نحاس وخارصين مغموسين في محلول حمض الكبيريتيك، فإنه نتيجة لحدوث التفاعل الكيميائي يحدُث سريان للتيار الكهربائي ويضيء المصباح.
- تغير لون الكاشف الكهربائي، مثال: يتغيّر لون الشاي المر (البني الغامق) إلى اللون الأصفر الفاتح عند إضافته إلى حمض الهيدروكلوريك أو محلول هيدروكسيد الصوديوم.
- ظهور ضوء، مثال: 2Mg+O2→2MgO
- عند إشعال المغنيسيوم في الهواء الجوي يحترق مُنتجاً ضوءاً نتيجة التفاعل.